Équipe B. Garmy-Susini / A-C. PRATS
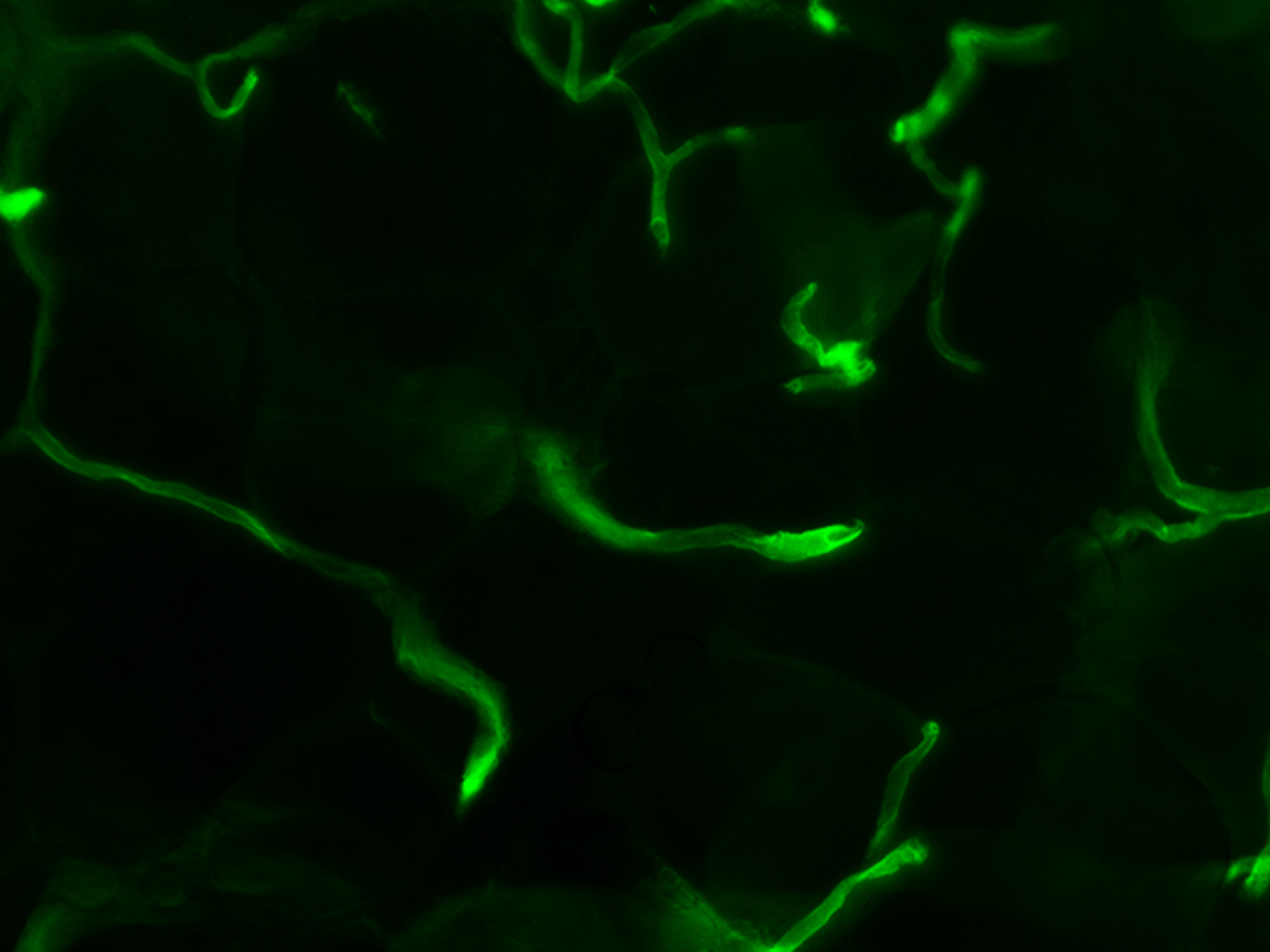
Régulations moléculaires des facteurs lymphangiogéniques dans les pathologies cardio-vasculaires
Le système lymphatique a pour rôle physiologique de collecter les fluides interstitiels, les graisses et les cellules immunitaires avant de rejoindre la circulation sanguine par le biais de la veine sous-clavière. En condition pathologique, une dysfonction du système lymphatique provoque la formation de lym-phoedèmes, une pathologie handicapante liée à une accumulation de tissu adipeux et de fluides dans les membres. Plus récemment, le rôle du système lymphatique a été identifié dans la fonction cardiaque. Ce système serait nécessaire pour prévenir et résorber les œdèmes cardiaques et pré-server le flux continu d’oxygène et de nutriments dans les tissus. Enfin, le système lymphatique représente le premier site métastatique des tumeurs solides et représente une cible prometteuse des thérapies anti-cancéreuses. L’ensemble de ces pathologies sont associées à des stress communs tels que le manque d’oxygène ou hypoxie, et le choc thermique qui induisent des changements majeurs de l’expression génique des facteurs (lymph)angiogéniques.Notre hypothèse de travail est que la restauration du drainage lymphatique dans les tissus lésés accélérera considérablement la guérison en améliorant l’homéostasie tissulaire, en régulant le trafic de cellules inflammatoires et en favorisant le drainage de l’œdème. Dans ce contexte, notre groupe se concentre sur les pathologies caractérisées par un dysfonctionnement lymphatique massif: lymphœdème secondaire et ischémie cardiaque. Notre objectif est d’associer des approches de recherche fondamentale et translationnelle dans le domaine de la biologie du lymphatique.
L’Équipe

Barbara GARMY-SUSINI

Anne-Catherine PRATS

Eric LACAZETTE

Florent MORFOISSE

Xavier CHAUFOUR

Julie MALLOIZEL-DELAUNEY

Hervé ROUSSEAU

Fatima MOKRANE

Aurélien HOSTALRICH

Elisa BALZAN

Ana ALVAREZ

Roxane SYLVESTRE

Géraldine PUEL

Morgane DO CARMO
Physiopathologie du lymphoedème
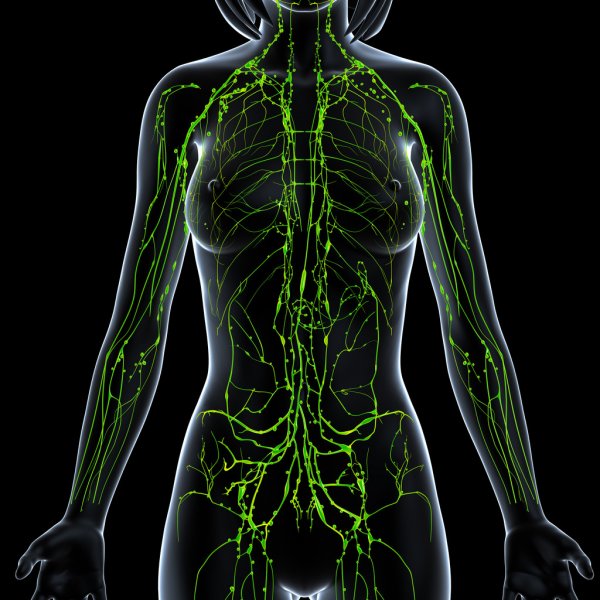
Coordinatrice : Barbara Garmy-Susini
Barbara Garmy-Susini étudie la physiopathologie du lymphœdème, une pathologie handicapante et douloureuse à ce jour incurable. Nous étudions à la fois les facteurs de risque et les biomarqueurs de la pathologie. À l’aide d’approches OMICS (lipidomique, RNAseq), nous avons identifié des cibles thérapeutiques potentielles pour restaurer le flux lymphatique dans un membre lésé. Notre groupe a souligné le rôle crucial de la résolution de l’inflammation dans le développement du lymphœdème. Le projet intitulé «Theralymph», financé par l’appel d’offre Européen H2020 va nous permettre de réaliser un essai clinique de phase I / II chez les patients ayant développé un lym-phoedème grâce à une technologie innovante basée sur les vecteurs à ARN. Nous étudions éga-lement comment le microenvironement fibrotique les lymphatiques peut aggraver le lymphoedème et le rendre irréversible.
Contrôle de la traduction et thérapie génique des pathologies cardiovasculaires
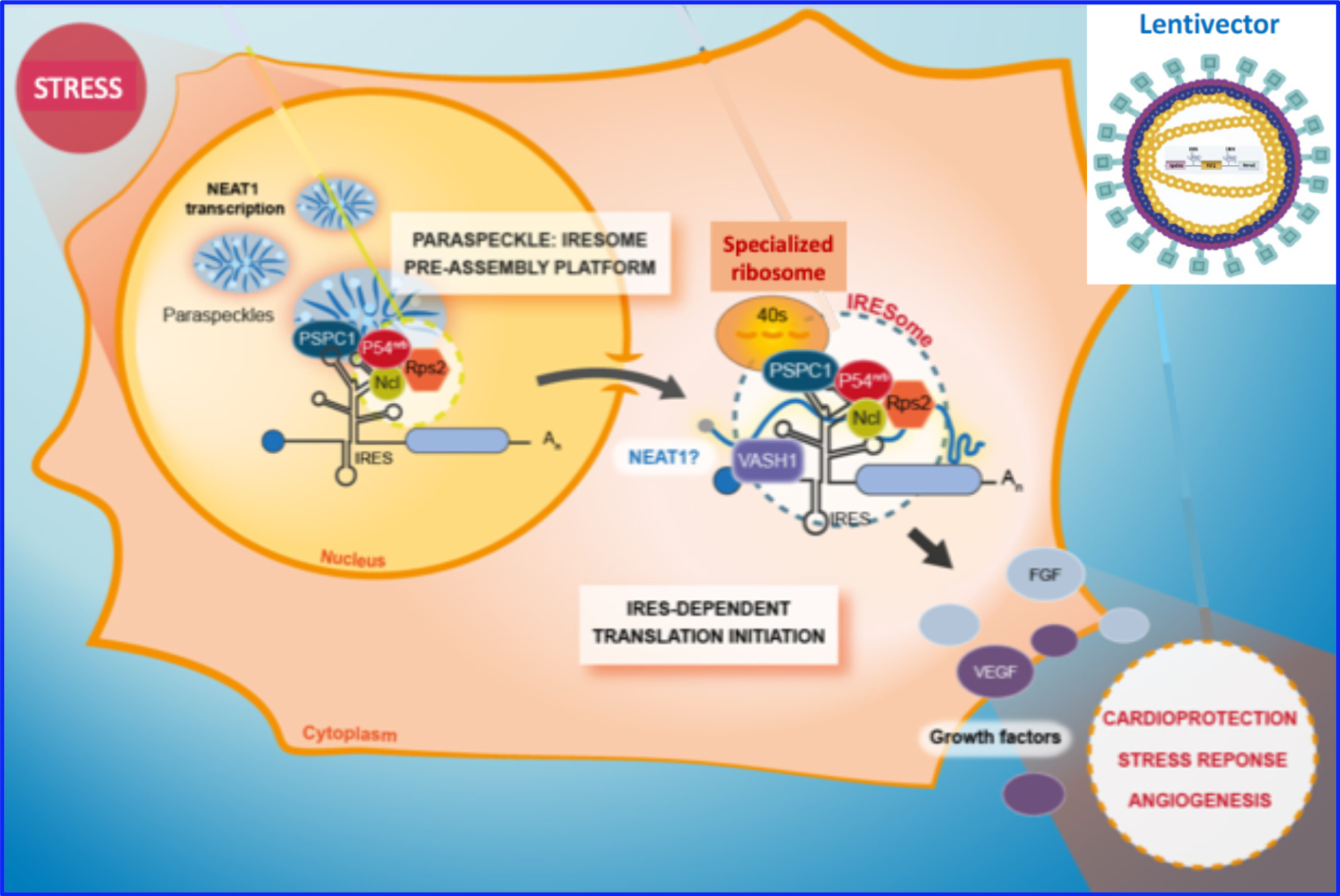
Coordinatrice : Anne-Catherine Prats
A.C. Prats étudie la régulation de la traduction des ARNm lors du stress cellulaire. Elle recherche des modifications de la machinerie de traduction conduisant à la formation de ribosomes spéciali-sés dans la traduction des ARNm contenant des IRES, structures activatrices de la traduction lors du stress. L’étude est menée dans les cardiomyocytes stressés et dans l’ischémie cardiaque, ainsi que dans les cellules endothéliales lymphatiques soumises à une chimiothérapie, facteur aggra-vant du lymphoedème. Ce projet aura un impact sur la compréhension du contrôle de l’expression génique dans les pathologies cardiovasculaires. A.C. Prats développe des approches translation-nelles de thérapie génique combinée à l’aide de lentivecteurs multicistroniques utilisant les IRES pour co-exprimer plusieurs molécules thérapeutiques. Elle contribue ainsi aux projets européens CARDIOPATCH et THERALYMPH.
ARN circulaires : biogenèse et fonctions dans la lymphangiogenèse.
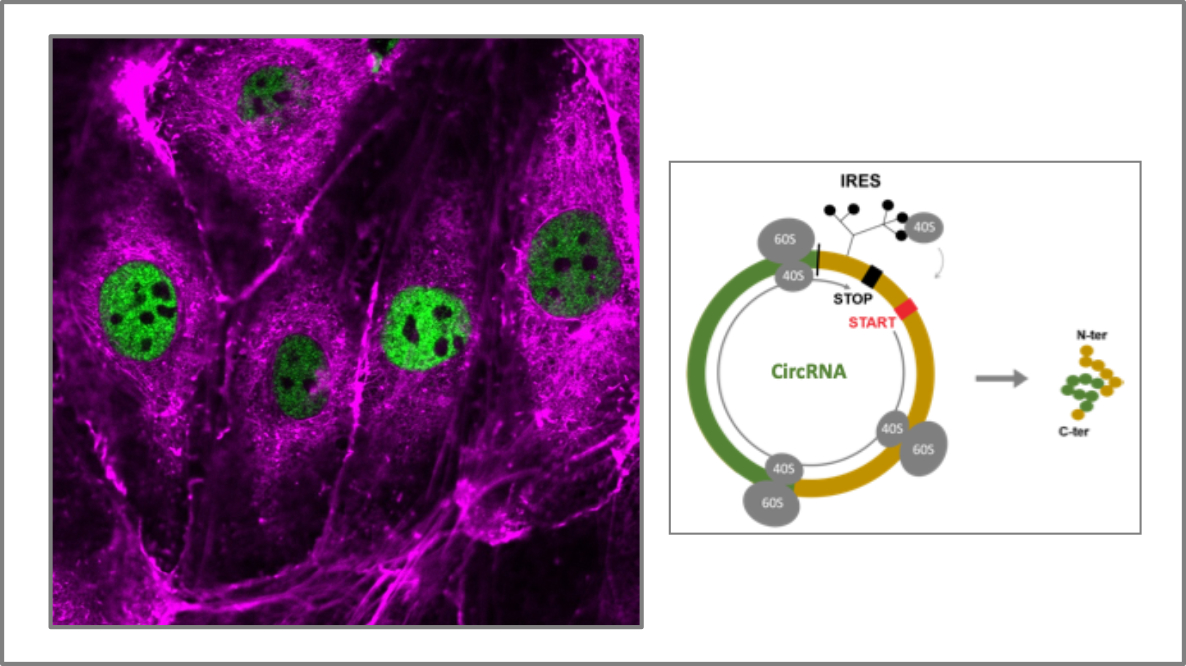
Coordinateur : Eric Lacazette
Eric Lacazette s’intéresse à caractériser et décrypter les fonctions d’une nouvelle famille d’ARN dans les cellules endothéliales lymphatiques : les ARN circulaires (circARN). Ces circARN sont identifiés par RNAseq adossé à une approche bio-informatique dédiée puis caractérisés fonction-nellement dans des modèles in-vitro et in-vivo. Nos travaux montrent que certains circARN sont traduits via un mécanisme d’initiation alternatif de la traduction et codent pour des protéines aux fonctions inconnues à l’heure actuelle. Les circARN participeraient ainsi aux mécanismes d’adaptation fine de l’expression génique des cellules endothéliales en fonction du microenviron-nement. Ce projet vise aussi à mieux percevoir l’impact des circARN en contexte physiopatholo-gique tel que le lymphœdème. Collaboration: C. Gaspin et J. Mariette (Unité de Mathématiques et Informatique Appliquées de Toulouse, INRAE).
RESLY : Etude de la RESolution de l’inflammation dans le LYmpheodème secondaire

Coordinatrice : Barbara Garmy-Susini
Projet financé par région Occitanie et les fonds FEDER
Contexte scientifique: Le système lymphatique est constitué d’un réseau de capillaires lymphatiques à paroi mince et de collecteurs qui drainent les liquides interstitiels, les lipides et les cellules immunitaires pour les ramener vers la circulation sanguine dans la zone jugulaire (Alitalo, K., 2005) . Un dysfonctionnement du réseau lymphatique induit des pathologies telles que le lymphoedème, les métastases tumorales et diverses maladies inflammatoires chroniques (Alitalo, K., 2011).
Le lymphœdème est un trouble du système vasculaire lymphatique caractérisé par un retour lymphatique altéré, un gonflement des extrémités par accumulation de tissu adipeux et fibrose dans les membres, ainsi qu’une inflammation chronique (Mortimer, P.S.2014). Le lymphoedème peut être héréditaire (primaire) ou survient après une infection ou le traitement d’un cancer (secondaire) et se caractérise par une inflammation chronique (Gardenier, J.C. 2015). Bien qu’il s’agisse d’une maladie invalidante et douloureuse, il n’existe à ce jour aucun traitement curatif.
Ce projet implique 2 laboratoires académiques publics, situés à l’I2MC (CHU Rangueil), dont l’un est expert dans le domaine des cellules endothéliales lymphatiques et l’autre dans le domaine du tissu adipeux humain ainsi qu’un partenaire industriel régional, la Société AMBIOTIS, expert dans la quantification et l’identification en spectrométrie de masse de molécules biologiquement actives appelées lipoxines, résolvines, marésines et protectines. Ce projet se divise en quatre principaux objectifs:
1/ Identifier les modifications de lipides inflammatoires impliqués dans la résolution de l’inflammation chez les patients atteints de lymphoedème secondaire (biosies appareillées).
2/ Evaluer l’effet de ces lipides inflammatoires sur la fonction endothéliale lymphatique (transport lymphatique des cellules immunitaires in vitro et in vivo)
3/ Valider les résultats dans un modèle pré-clinique de lymphoedème
4/ Intervenir par une approche ciblée pour favoriser la résolution et régénérer la circulation lymphatique dans le membre lésé.

publications
15-Lipoxygenase promotes resolution of inflammation in lymphedema by controlling Treg cell function through IFN-β. Zamora A, Nougué M, Verdu L, Balzan E, Draia-Nicolau T, Benuzzi E, Pujol F, Baillif V, Lacazette E, Morfoisse F, Galitzky J, Bouloumié A, Dubourdeau M, Chaput B, Fazilleau N, Malloizel-Delaunay J, Bura-Rivière A, Prats AC, Garmy-Susini B. Nat Commun. 2024. Pubmed
Apelin-VEGF-C mRNA delivery as therapeutic for the treatment of secondary lymphedema. Creff J, Lamaa A, Benuzzi E, Balzan E, Pujol F, Draia-Nicolau T, Nougué M, Verdu L, Morfoisse F, Lacazette E, Valet P, Chaput B, Gross F, Gayon R, Bouillé P, Malloizel-Delaunay J, Bura-Rivière A, Prats AC, Garmy-Susini B. EMBO Mol Med. 2024. Pubmed
Specific Circular RNA Signature of Endothelial Cells: Potential Implications in Vascular Pathophysiology. Diallo LH, Mariette J, Laugero N, Touriol C, Morfoisse F, Prats AC, Garmy-Susini B, Lacazette E. Int J Mol Sci. 2024. Pubmed
Coordinating Effect of VEGFC and Oleic Acid Participates to Tumor Lymphangiogenesis.
Sex Hormones in Lymphedema. Morfoisse F, Zamora A, Mar-chaud E, Nougue M, Diallo LH, David F, Roussel E, Lacazette E, Prats AC, Tatin F, Garmy-Susini B.. Cancers 2021. Pubmed
ILS NOUS SOUTIENNENT









Inserm/UPS UMR 1297 - I2MC Institut des Maladies Métaboliques et Cardiovasculaires
1 avenue Jean Poulhès - BP 84225 - 31432 Toulouse Cedex 4
Tél. : 05 61 32 56 00
Horaires
Du lundi au vendredi
8h30 - 12h30 / 13h45 -16h45